Un nouvel espoir contre les cancers de l’os
Actualité
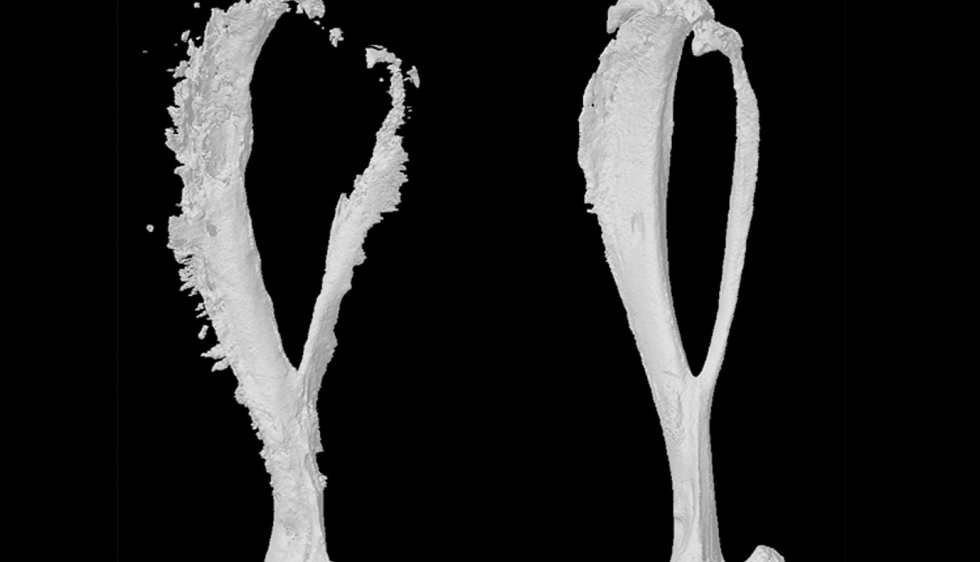
Des chercheurs nantais ont développé une nouvelle stratégie pour stopper la progression tumorale chez les enfants atteints d’un cancer des os.
Touchant principalement les enfants et les adolescents, les cancers primitifs de l’os affichent des taux de survie à 5 ans de 50 à 70 % dans les meilleurs cas, un pronostic qui n’a pas évolué au cours des trente dernières années malgré l’évolution des traitements par chimiothérapie. Bien qu’ayant des causes diverses et encore mal connues, ces cancers, qu’il s’agisse de l’ostéosarcome ou du sarcome d’Ewing, semblent engendrés par des dysfonctionnements cellulaires similaires à ceux qui sont à l’origine de la fragilisation des os (lésions, fractures...). « Nous savons en effet que la libération de grandes quantités de “facteurs de croissance” dans l’environnement osseux provoquée par les cellules tumorales perturbe l’équilibre entre l’action des cellules constructrices (ostéoblastes) et destructrices (ostéoclastes) du tissu osseux », explique François Lamoureux, chercheur contractuel Inserm de l’unité 957 Physiopathologie de la résorption osseuse et thérapie des tumeurs osseuses primitives.
Des dégradations de l’os
L’excès de ces facteurs de croissance induit une surproduction d’ostéoclastes entraînant, non seulement d’importantes dégradations de l’os, mais également la libération d’autres facteurs de croissance emprisonnés dans la matrice osseuse. « Or, plus la quantité de facteurs de croissance dans le microenvironnement de la tumeur est importante, plus la tumeur prolifère, soulignent Benjamin Ory, maître de conférences à l’Université de Nantes, et Marc Baud’huin, assistant hospitalo-universitaire au CHU de Nantes, tous deux chercheurs au sein de la même unité Inserm. Aussi, nous avons cherché un moyen de stopper ce cercle vicieux, en agissant sur ses trois composantes : la tumeur, les ostéoclastes et les ostéoblastes, et de rétablir ainsi l’équilibre entre destruction et formation de l’os. »
Des gènes facilitateurs
L’équipe nantaise s’est alors intéressée à l’action d’une protéine (la protéine à bromodomaine BRD4) connue pour participer à la régulation de l’expression de gènes. « Nous avons remarqué que cette protéine avait tendance à se fixer sur des gènes dits “facilitateurs de tumeurs”, précisent-ils. Pour inhiber la progression de la tumeur, il nous fallait donc trouver un moyen de l’empêcher de se fixer sur ces gènes. » Pour ce faire, ils ont découvert, au cours de recherches bibliographiques, une molécule chimique (JQ1), synthétisée par un chercheur de Harvard, dont l’efficacité pour bloquer BRD4 avait été validée dans le cas de lymphomes et de leucémies. Ils ont alors décidé de tester ensemble son efficacité contre les tumeurs osseuses en l’insérant au niveau du site de fixation de BRD4. Au bout de trente-cinq jours de traitements par injection de la molécule JQ1, ils ont constaté une diminution de 50 % du volume de la tumeur chez les souris traitées par rapport à celles non traitées. De plus, les os des souris traitées montraient une architecture normale, organisée et sans lésion apparente. « Nous nous sommes ainsi aperçus que JQ1 bloque non seulement la prolifération tumorale mais également la surproduction des ostéoclastes », expliquent les trois chercheurs qui travaillent désormais à transformer cette preuve de concept en un nouveau traitement des cancers osseux primitifs, des métastases osseuses et peut-être même d’autres pathologies comme l’ostéoporose.
François Lamoureux Tél. 02 40 41 28 98
francois.lamoureux [at] univ-nantes.fr (francois[dot]lamoureux[at]univ-nantes[dot]fr)
TOUTES LES ACTUALITÉS
du magazine Sciences Ouest






