Localiser sans a priori
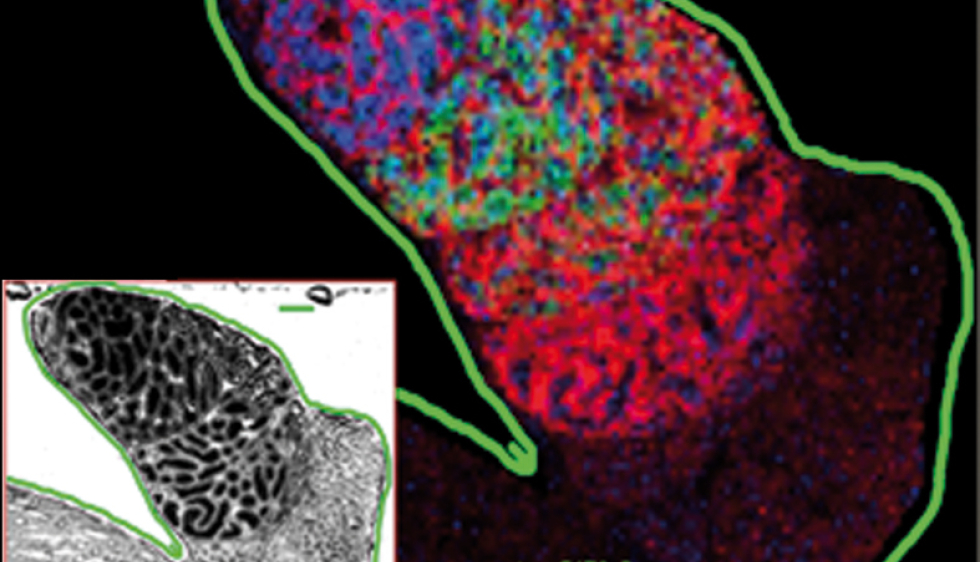
Basée sur le laser, une méthode d’imagerie bouleverse la recherche dans le domaine du vivant. Des Rennais la maîtrisent.
Une jolie lumière fluorescente, rien de tel pour se faire repérer ! Pour localiser une molécule dans une cellule ou un tissu, les chercheurs utilisent couramment des anticorps associés à un composé fluorescent. Cela donne de très bons résultats, mais nécessite de connaître la molécule que l’on souhaite localiser. Car les anticorps doivent être dirigés contre quelque chose. Une nouvelle méthode offre une alternative : il s’agit de l’imagerie Maldi.
Chercher n’importe quelles molécules
La technologie est basée sur la spectrométrie de masse qui consiste à irradier avec une lumière laser des échantillons de tissus très fins et préalablement recouverts d’une matrice spéciale, pour provoquer une réaction d’ionisation. Ce n’est pas une intensité lumineuse qui révèle ici les molécules d’intérêt, mais la mesure de leur masse(1). « Cette technologie permet de localiser sans a priori et sans marquage tous types de molécules », explique Mélanie Lagarrigue, postdoctorante au sein de la plate-forme protéomique Protim dirigée par Charles Pineau, à l’Irset(2). La localisation est proche du niveau cellulaire et les spectromètres de masse les plus performants permettent désormais d’associer très facilement la masse détectée à une molécule quand celle-ci est petite, comme les pesticides. « Pour les plus grosses molécules comme les protéines, c’est plus compliqué. On est obligé d’utiliser parallèlement les méthodes d’extraction et d’identification classiques et de faire des recoupements », précise-t-elle.
Le pesticide des bananeraies
Mise au point en 1997 par un chercheur américain, l’imagerie Maldi est de plus en plus utilisée dans les laboratoires et peut s’appliquer à des domaines très variés. En cancérologie, elle permet d’identifier de nouveaux biomarqueurs pour suivre, de façon précoce, le développement d’une tumeur. En pharmacologie, elle peut éviter de manipuler des molécules radioactives, autre méthode de marquage couramment utilisée, notamment dans les phases d’étude de pharmacocinétique, pour suivre le devenir du principe actif d’un médicament dans l’organisme. Le même principe peut être utilisé en toxicologie : Mélanie Lagarrigue et ses collègues de l’Irset ont récemment mis au point une technique de quantification du chlordécone(3), un pesticide anciennement employé dans les bananeraies. « Nous avons déterminé son profil d’accumulation au cours du temps dans des foies de souris tout en préservant l’information de localisation, précise-t-elle. De même, nous travaillons sur la biodistribution du bisphénol A, un possible perturbateur endocrinien, dans le testicule humain. » Et pour suivre efficacement ces composants de petite taille, la plate-forme rennaise a fait l’acquisition, l’été dernier, d’un nouvel appareil : un spectromètre de masse à très haute résolution(4).
Passage à la 3D
Enfin, toujours à la pointe de l’innovation, l’équipe de Charles Pineau fait partie d’un grand consortium international qui planche sur le développement d’un outil d’imagerie Maldi en trois dimensions, où le volume est reconstruit à partir de la superposition des coupes en deux dimensions. Un projet phare, dans lequel les Rennais seront bien repérés.
(1) C’est l’intensité du rapport masse sur charge (m/z) des molécules qui est enregistrée en chaque point.
(2) L’Irset, Institut de recherche en santé, environnement et travail, est une Unité mixte de recherche Inserm, Université de Rennes 1, École des hautes études en santé publique (Ehesp), en association avec l’Université des Antilles et de la Guyane, le CNRS et les CHU de Rennes et Pointe-à-Pitre.
(3) Lire La reproduction sous toxiques dans Sciences Ouest n° 330, avril 2015.
(4) Grâce à sept cofinancements.
Mélanie Lagarrigue
Tél. 02 23 23 72 63
melanie.lagarrigue [at] univ-rennes1.fr (melanie[dot]lagarrigue[at]univ-rennes1[dot]fr)
TOUT LE DOSSIER
du magazine Sciences Ouest






